亜鉛情報about zinc
亜鉛による防食
1.腐食とは
腐食とは、金属材料が、その周囲の環境と反応して消耗する現象を指し、水が関与する湿食と水が関与しない乾食の2種類があります。
1-1)乾食と湿食
乾食は、高温の空気や腐食性ガスによる酸化が原因で発生し、高温酸化とも呼ばれます。一方、湿食は、水、海水、地中などの電気を通す環境下で、電子やイオンが関与する電気化学反応によって生じる腐食現象を意味し、常温でも起こります。 我々が身近で見ることが出来る腐食の殆どはこの湿食で、当社のZAPシリーズも湿食を対象とした防食材です。 以下の説明は全て湿食を対象としています。
1-2)全面腐食と局部腐食
さらに湿食は、全面腐食(均一腐食)と局部腐食に分類されます。全面腐食は、金属材料、腐食環境何れも均質な場合に見られ、全面が均一 に腐食するため、その進行速度は遅く鉄では最大でも0.1mm/年程度です。一方、局部腐食は金属材料側あるいは腐食環境が不均一な場 合見られ、部分的に腐食が集中するため、腐食深さは深く同時に進行速度も速くなる傾向があり、早期に重大な事故に繋がる場合もあります。
金属材料側、腐食環境側の不均一には次のようなケースがあります。
- 金属材料側の不均一:組織、化学成分、析出物、結晶方位、転位密度、残留応力の差、結晶粒界と粒内、酸化物の有無や厚さの差など
- 腐食環境側の不均一:溶存酸素濃度、イオン濃度、液温、流速、外部応力の差、付着物の有無など
1-3)ミクロ腐食電池とマクロ腐食電池
ミクロ腐食電池とは 4-1)-a)「電気防食のメカニズム」も参照
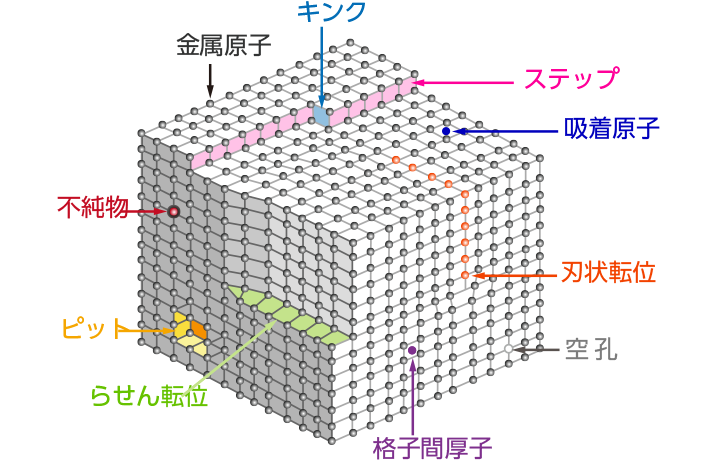
金属表面は、外観では均質に見えても右図に示すように転位、ステップ、キンク、不純物など原子配列の乱れた欠陥が不可避的に多数あり、微視的には不均質な状態にあります。
欠陥部やその周囲の原子は、活性で高いエネルギー状態にあるため、バルクから飛び出し、系のエネルギーを下げるよう振る舞います。
このため腐食環境下では、これら欠陥部の原子が飛び出しアノードとして働き、その周囲をカソードとしてミクロな局部電池が形成されますが、この原子サイズオーダーのアノード、カソードによる腐食電池をミクロ腐食電池(ミクロセル)と言います。
欠陥部から原子が飛び出し消失すると、次はその隣接原子が不安定となり飛び出します。
このようにアノードが、1箇所に固定されることなく次々と移動し、しかもアノードとなる活性点は分散して無数にあるため、腐食はアットトランダムに生起し、結局均一な腐食形態(全面腐食)となります。
マクロ腐食電池とは
マクロ腐食電池(マクロセル)とは、異種金属接触腐食や隙間腐食のようにアノード、カソードの位置が固定され、サイズも目で確認出来る大きさを有する腐食電池を指します。
腐食はミクロ腐食電池を基本とし、アノード、カソードが固定されるなど条件が揃った時マクロ腐食電池もミクロ腐食電池に重畳して形成され、腐食が進行します。
下表にマクロ腐食電池、ミクロ腐食電池の特長を示します。
マクロ腐食電池・ミクロ腐食電池の特長
| 項目 | ミクロ腐食電 | マクロ腐食電池 |
|---|---|---|
| サイズ | 原子サイズのオーダー | 巨視的サイズ |
| アノードの位置 | アノードの位置は移動する | アノード、カソードの位置は固定 |
| 腐食形態 | 全面腐食(均一腐食) | 局部腐食 |
| 腐食の程度 | 腐食は軽微 | 腐食はミクロ腐食電池より酷くなる傾向がある |
1-4)金属と錆
金と白金族金属(白金、ロジウム、パラジウム等)を除くと、鉄、アルミニウムなど多くの金属は、天然には鉱石として最も安定なの形(主に酸化物)で存在しています。人間は、鉱石を採掘し精錬することで、無理矢理鉱石から酸素を取り除き、化学的に不安定な純度の高い金属にして活用しています。このため金属は、水分や酸素の多い環境下に曝されると容易に元の化学的に安定な酸化物に戻ろうと錆が発生し、結局もとの鉱石の形に帰ります。従って、この腐食を避け設備の機能を維持するためには、電気防食や塗装など何らかの防食処理が必須となります。
2.腐食のメカニズム
2-1)腐食は電池反応
一般に湿食は、金属材料中の原子が電解質水溶液中に陽イオンとして溶け出すアノード反応(酸化反応)と、酸化剤が電子を受け取るカソード反応(還元反応)が対をなして同時に起こる局部的な電池反応です。この時流れる電流は、アノードがカソードより低電位となるため金属表面のカソードからアノード、電解質溶液、カソードと流れます。
金属材料が、腐食するにはこのアノード反応とカソード反応の組み合わせが絶対条件で、どちらか片側が止まれば腐食は停止し、片側の速度が低下すれば腐食速度も低下します。
また金属材料が、湿食によって腐食するためには水(電解質水溶液)と酸化剤が不可欠で、そのいずれかが欠けると腐食することはなく、砂 漠、極寒地、無酸素の環境下では腐食しません。なお酸化剤としては中性の水中ではO2が、酸性溶液中ではH+やO2が主に働きます。
2-2)水滴における腐食
今、鉄板上の水滴(中性)で腐食の状態を模式図で示すと、下図となり、中央部には腐食による凹部が、その周辺に腐食生成物の堆積が見られます。これを例に腐食メカニズムを以下説明します。
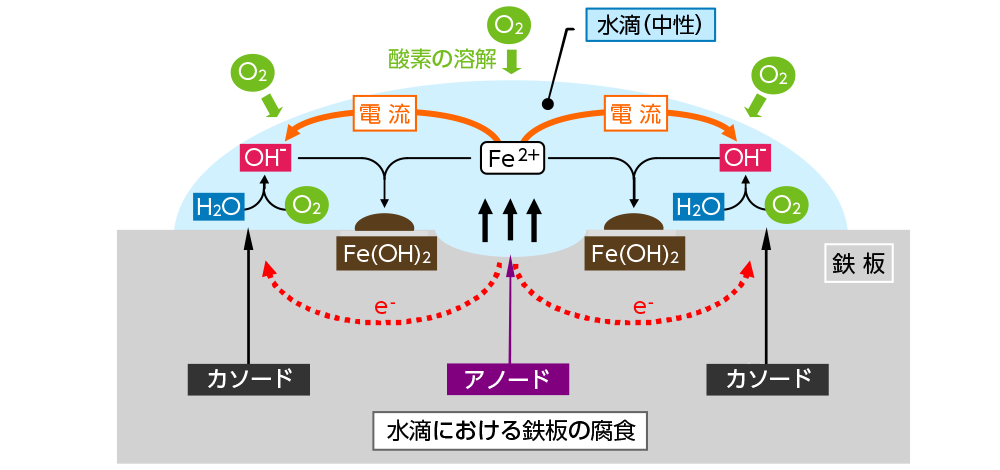
相対的に水滴が厚く酸素濃度が低い水滴中央(アノード部)では、<1式>のように鉄原子(Fe)は、鉄板に電子(e−)を残し第一鉄イオン(Fe2+)の形で溶解し、液中に拡散します。
一方、酸素濃度の高い水滴周辺(カソード部)では、<2式>のように水(H2O)、酸素(O2)、及び<1式>の鉄溶解部から供給される電子(e−)が反応し水酸化イオン(OH−)を生じます。
次にpH4程度の酸性溶液中では、酸化剤として溶液中の水素イオン(H+)が酸素(O2)と共に機能するので、アノード、カソードの各反応は下記の通りとなります。溶液のpHが低いほどカソード反応として<4式>式の水素ガス発生反応が支配的となります。
3.種々な腐食
腐食を湿食、乾食に分け記載すると下表になります。
| 分類 | 説明 | 観察例 | ||||
|---|---|---|---|---|---|---|
| 腐 食 |
湿 食 |
全面腐食 (均一腐食) |
腐食環境に暴露される面が、ほぼ均一に腐食する現象 | ・塩酸等酸液中の鋼板 ・大気、淡水など中性環境中の鋼板 |
||
| 局 部 腐 食 |
濃淡電池腐食 | 腐食環境の一部に濃度差(塩分や酸素濃度等)がある場合に見られる腐食現象 (酸素濃度に依るものを特に通気差腐食と言う) |
・給水配管中の錆瘤の下部 ・照明灯ポールなどの地際 ・水線腐食 |
|||
| 隙間腐食 | 上記の濃淡電池に起因し、10μm程度の極めて狭い隙間で生じる腐食現象(濃淡電池腐食の一種) | ・SUS製フランジのガスケット部 ・ボルトナット締付部 |
||||
| 異種金属接触腐食 (ガルバニック腐食) |
海水など導電性のある電解質溶液中で種類の異なる金属が電気的に接触すると、両者間のイオン化傾向の差により電位差が生じ腐食が進展する現象 | ・鋼板まで達する傷を有するブリキ板 ・SUSバルブと鋼管からなる配管系 |
||||
| 孔食 | 不働態被膜の破壊部など金属表面の局部だけに腐食が集中、進展し、孔状になる現象 | ・海水中のアルミ板 ・SUS304系熱交換チューブ内面 |
||||
| 溝状腐食 | 配管の溶接部などが、溝状に優先的に腐食する現象 | ・海水、工業用水に使用される電縫鋼管 | ||||
| 粒界腐食 | 金属の結晶粒界は元素の偏析や化合物の析出が起こり易い為、粒内に比べ腐食され易くなる現象 | ・鋭敏化した304系ステンレス板 ・金属組織観察時のエッチング処理 |
||||
| 微生物誘起腐食 (MIC) |
ある種の微生物の活動によって腐食が促進する現象 | ・硫酸塩還元菌を含む土中の鋼管 ・SUS304製ボイラ給水管の溶接部 |
||||
| 脱成分腐食 (選択腐食) |
合金の成分の一部が選択的に溶出する腐食現象 | ・海水を使用する黄銅製コンデンサ管 | ||||
| 応力腐食割れ | 特定の腐食環境下では、降伏点以下の低い引張応力下でも腐食により割れが発生する現象 | ・塩素イオンを含む冷却用SUS304系配管 ・高温高濃度NaOH溶液中の鋼 |
||||
| 腐食疲労 | 腐食環境下で繰り返し応力が作用する時に生じる破壊現象 | ・振動を伴う冷却水熱交チューブ | ||||
| エロージョン・コロージョン (摩耗損傷、潰食) |
腐食性の流体による電気化学的腐食だけでなく、流体中の流動する水、土砂などによる機械的摩耗作用が伴う現象 | ・配管用エルボ、T字管の下流部 ・オリフィス計の下流部 |
||||
| 迷走電流腐食 (電解腐食、電食) |
地中、水中で本来通るべき回路以外の金属体に電流が流入し(迷走電流と言う)、それが地中、水中に再び流出するときに生じる腐食現象 | ・鉄道近くの地下埋設鋼管や鋼製設備 | ||||
| 乾 食 |
高温酸化 | 高温で大気、酸素、水蒸気、炭酸ガスで酸化する現象 | ・鋼製遮熱板 ・輸送機器のエキゾーストマニホールド |
|||
| 高温がス腐食 | 塩素、塩酸、硫化水素などの腐食性ガスで腐食する現象 | ・化石燃料の燃焼ガスに接するボイラ管 ・石油精製プラントの加熱炉管 |
||||
a) 隙間腐食に対する亜鉛の効果
隙間腐食のメカニズム
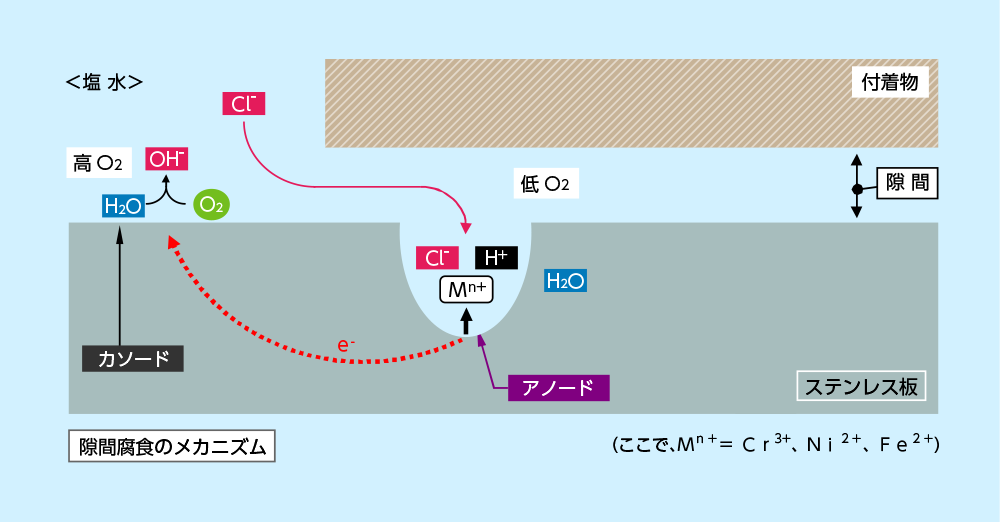
塩水中のステンレス板を例に隙間腐食を説明します。
図のように金属材料上に10μmオーダの隙間が存在すると、その隙間内外で酸素濃度の差が生じるため酸素濃淡 電池が形成され隙間内部が腐食します。しかしこの環境下でもステンレスは、塩素イオン(Clー) を含まない水であれば不働態皮膜の防食作用によって腐食しませんが、塩素イオンが存在すると不働態皮膜が局所的 に破壊されるため、クロムイオン(Cr3+)、ニッケルイオン(Ni2+)、鉄イオン(Fe+2)が溶解し、軽微な 孔食がまず生じます。
この軽微な孔食が一端生じると、下記要因により孔食内での不働態形成が不可能となり、また周囲のカソードの面積に 比べ孔食面積が小さいため腐食が、集中し、やがて深い孔食に至ります。
- 塩素イオン(Clー)が電気泳動で孔食内に運ばれ、塩素イオン濃度が増大する
- 溶解したクロムイオン(Cr3+)、ニッケルイオン(Ni2+)、鉄イオン(Fe2+)は、孔食内外で液交換し難いため孔食内に滞留し、孔食内の水との加水分解反応で水素イオンが発生し、孔食内のpHは低下し強い酸性となる
下記にCr3+の場合を示します。
Cr(OH)2+ + H2O → Cr(OH)2+ + H+
Cr(OH)2+ + H2O → Cr(OH)3 + H+
実例

塩水中に2000hr浸漬していたSUS430板で観察された隙間腐食(断面写真)

SUS316L製の海水用配管フランジで観察された隙間腐食。腐食深さは、最大A部で2.08mmに達していました。
亜鉛の効果
ZAPシートの技術資料の『5.ステンレス板の隙間腐食に対するZAPシートの効果』の実験に見られるように、亜鉛によって隙間腐食は防止できます。
b) 溝状腐食に対する亜鉛の効果
メカニズム
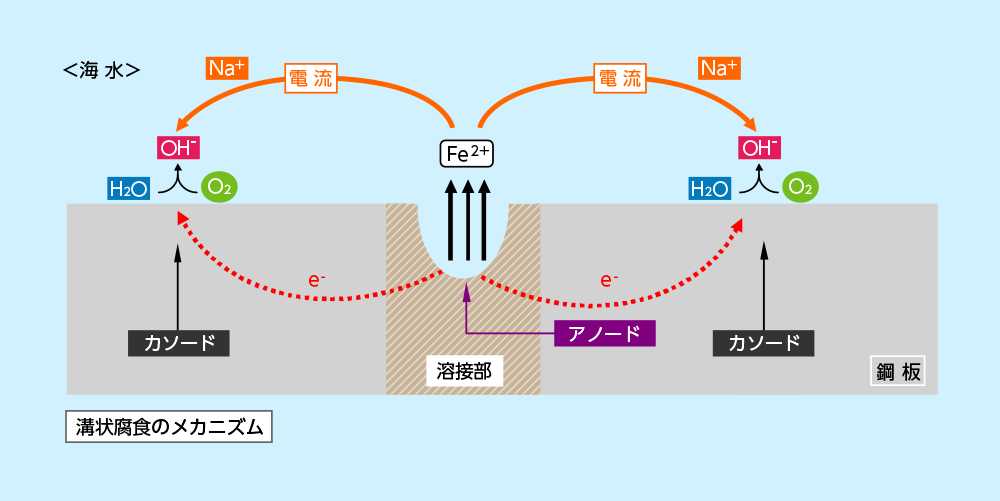
図に示すように溶接した鋼板では一般に溶接部が、アノード、その周囲がカソードとなり、腐食が溶接部に沿って溝状に集中的に発生します。これは、溶接部が溶接時の加熱、冷却により母材とは違った金属組織、化学成分を有す る結果、異なった電気化学的特性を帯びるためです。
実例
ブラスト処理した溶接鋼管を塩水噴霧試験(JIS Z2371に準拠) で2000hr暴露した時に見られた溝状腐食で、溶接部の腐食深 さは最大1.29mmであった。

亜鉛の効果
下記のZAPシリーズの技術資料に見られるように、ZAPテープ、ZAPペースト、ZAPーSUS、ZAPシート何れのZAPシリーズでも亜鉛の効果によって溝状腐食は防止できます。
c) 異種金属接触腐食に対する亜鉛の効果
異種金属接触腐食とは
異種金属接触腐食(galvanic corrosion)は、ガルバニック腐食や接触腐食とも呼ばれ、海水など導電性のある電解質溶液中に種類の異なる金属が電気的に接触している時に、卑な金属の腐食が通常に比べ加速される現象のことを言います。
従って異種金属接触腐食が生じるには、2種以上の金属が電気的に接触し電解質溶液中に存在し閉回路を形成することが必須で、いずれかが欠けると異種金属接触腐食は生じません。
また亜鉛、アルミニウム、マグネシウムなど腐食電位の低い合金を使った流電陽極による防食は、この異種金属接触腐食現象を積極的に利用した防食方法と言えます。
メカニズム
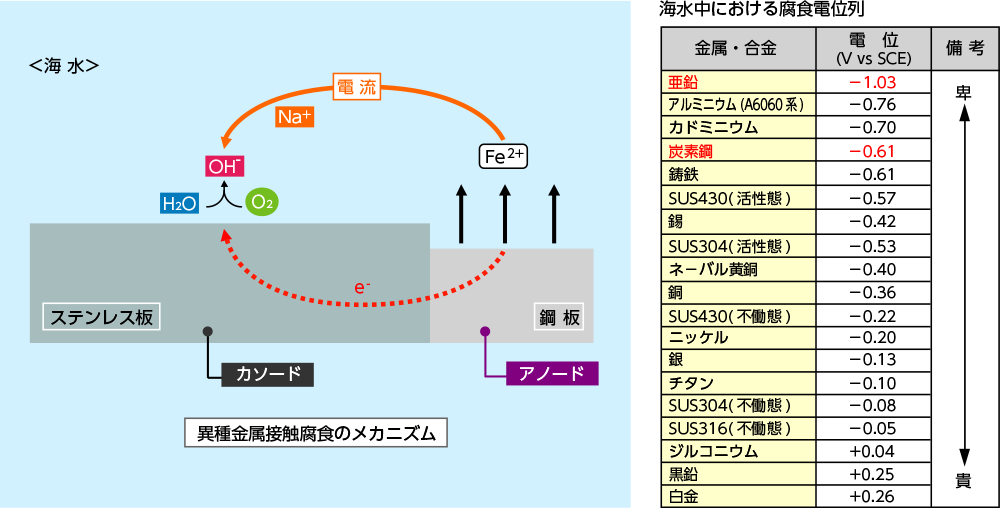
下表は、海水中における金属の腐食電位の序列(腐食電位列と言う)を示したもので、亜鉛のように電位の低い、卑な金属ほど高いイオン化傾向を有し、イオンになりやすいと言えます。
今、下図のように不働態化しているステンレス板と鋼板を電気的に接触させ海水中に浸漬した場合、ステンレス板に比べイオン化傾向の高い鋼板のみが溶出し、ステンレス板は全く腐食しません。
アノードである鋼板では、次の反応によるFe2+と海水中のNa+等がカソードであるステンレス板に向かって移動します。
一方、カソードでは海水中の溶存酸素が原動力となり、次の反応で生じたOHーイオンと海水中のClーイオン等がアノードに向かって電気泳動します。
このようにして電流が鋼板からステンレス板に流れ、閉回路が形成され異種金属接触腐食が進行します。
異種金属接触腐食に対する影響因子
異種金属接触腐食の程度は、主に次の因子により影響を受け変動します。
1.金属間の電位差
異種金属接触腐食は、金属間の腐食電位の差を駆動力として生じるため、その電位差の大きさで異種金属接触腐食の促進傾向を読み取ることができ、一般的には電位差が大きいほ ど腐食が促進される傾向が強くなります。
また目安として電位差が100mV以下であれば異種金属接触腐食の危険性は軽減されます。
2.金属の面積比
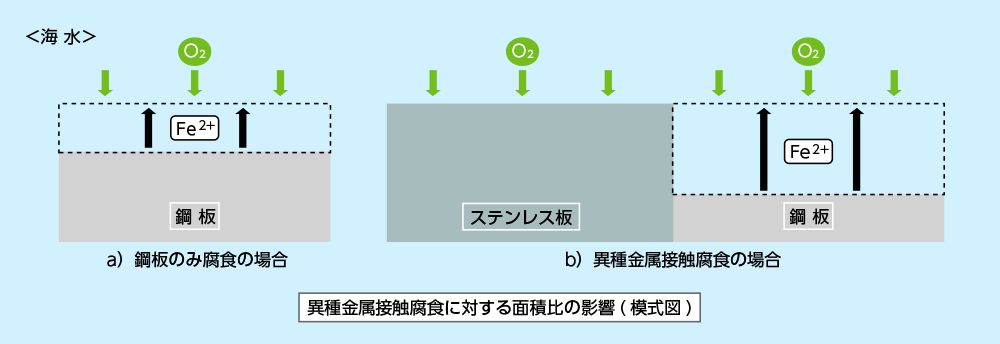
下図の示すように鋼板、ステンレス板の面積Sは同一で、鋼板が単独で海水中の浸漬されている場合(a)とステンレス板と電気的に接触して異種金属接触腐食が生起している場合(b)について説明します。
- a)の場合では、鋼板が均質な状態であっても原子サイズオーダーの不均一性によって、ミクロ腐食が上記のアノード反応〈1式〉、カソード反応〈2式〉によって鋼板の至る所で生起し、均一腐食します。
この時、腐食速度は鋼板表面に到達する溶存酸素量で律速されます。 - 一方、b)の場合では、異種金属接触腐食作用によりアノード反応(上記の〈1式〉)は鋼板のみで生じます。
しかし腐食速度を律速する溶存酸素のカソード反応は、鋼板表面だけでなくステンレス板表面でも起 こり、結局カソード反応は、鋼板とステンレス板の表面積が同一のため、a)の場合の2倍になります。
このため鋼板の腐食量も、2倍となり腐食が促進されます。
ステンレス板の面積が、鋼板の2倍であれば鋼板の腐食は3倍になります。 - 従って海水や淡水中の腐食のように酸素拡散支配型腐食では、卑な金属に対する貴な金属の面積比が大きいほど異種金属接触腐食によるダメージは大きくなります。
- このようにカソード反応、アノード反応の生じる面積比の生じる面積比によって腐食速度が決まる原理を「エバンスの補足面積の原理(catchment area principle))」と呼び、次式が成立します。

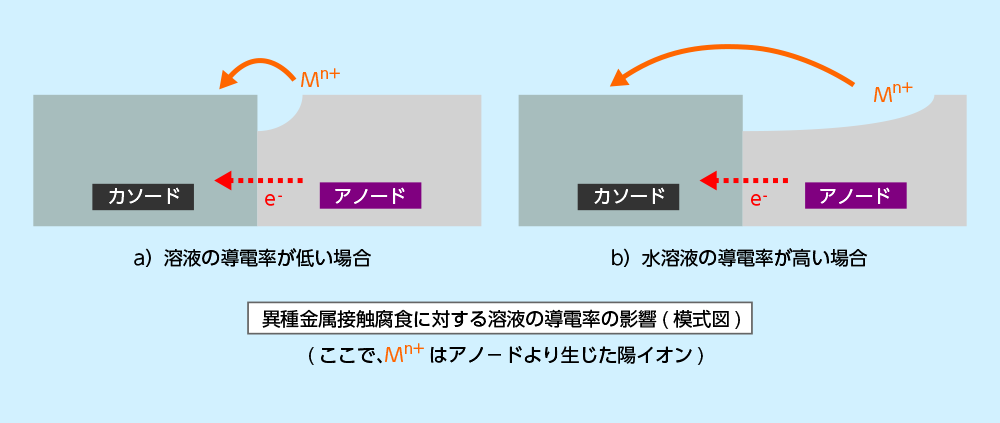
下図に示すように電解質溶液の導電率が高いほど、金属の接触部から遠い箇所まで異種金属接触腐食の影響が及びます。
右表に色々な液体の導電率を示しますが、塩化物イオン、ナトリウムイオン、硫酸イオンなどの電解質を多量に含む海水は、河川の約500倍電気を通すことが判ります。
海水や塩水のような電気抵抗の低い電解質水溶液中では、異種金属接触腐食が数メートル以上も離れた金属間で生じることがあるので、注意が必要です。
| 液体 | 導電率(mS/m) |
|---|---|
| 超純水 | 0.005 |
| 蒸留水 | 0.1 |
| イオン交換水 | 0.1 |
| 河川 | 11 |
| 水道水 | 19 |
| 地下水 | 26 |
| 0.5%塩水 | 880 |
| 海水 | 5000 |
| 5%塩水 | 7330 |
4.分極特性
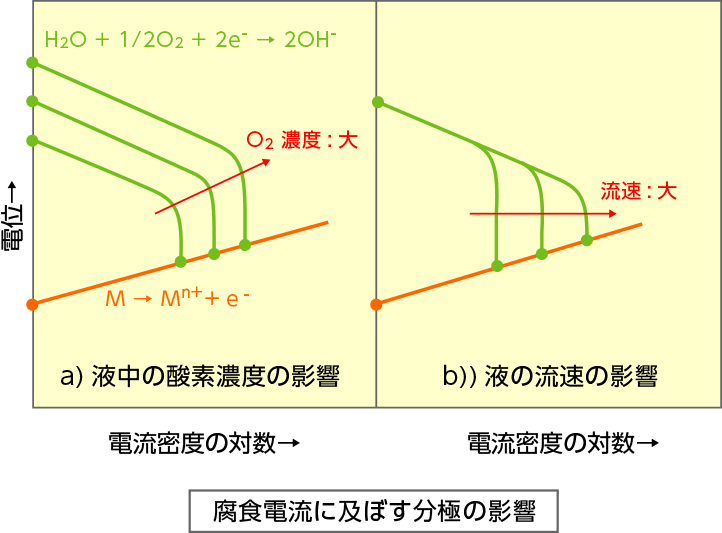
液体中で示す金属の平衡電位と実際の腐食時に観察される腐食電位との差を分極と呼びますが、異種金属接触腐食は、アノード分極、カソードの分極により影響を受けます。
分極への影響因子としては、濃度、温度、流速、及び酸性液中では水素過電圧などがあります。
例えば右図の分極図でカソード分極の影響を示すと、液中の溶存酸素が増加するとカソード反応が活発になるため腐食速度がアップします。
同様に流速が増加すると酸素の供給が増加するため腐食が加速されます。
異種金属接触腐食の実例
| 組み合わせ | 環境 | 現象 |
|---|---|---|
| 鋼板に締め付けられたアルミニウム製ネジ | 沿岸地域の構造物 | アルミニウム製ネジが腐食 |
| ステンレス屋根に取り付けられた銅製の避雷針 | 海岸近傍 | ステンレスが活性状態にあったためステンレス屋根に穴あきが発生 |
| 鋼管に取り付けられた青銅製バルブ | 沿岸で工業地域の配管 | 接触部の鋼管に局部腐食が発生 |
| 鉄製埋設管とコンクリート中の鉄筋 | 地中 | コンクリート中の鉄筋は不働態皮膜が発生し安定化するため埋設管が腐食 |
| 銅板屋根を鉄製の釘で固定 | 工業地帯 | 鉄製の釘に腐食が発生 |
実験による再現例
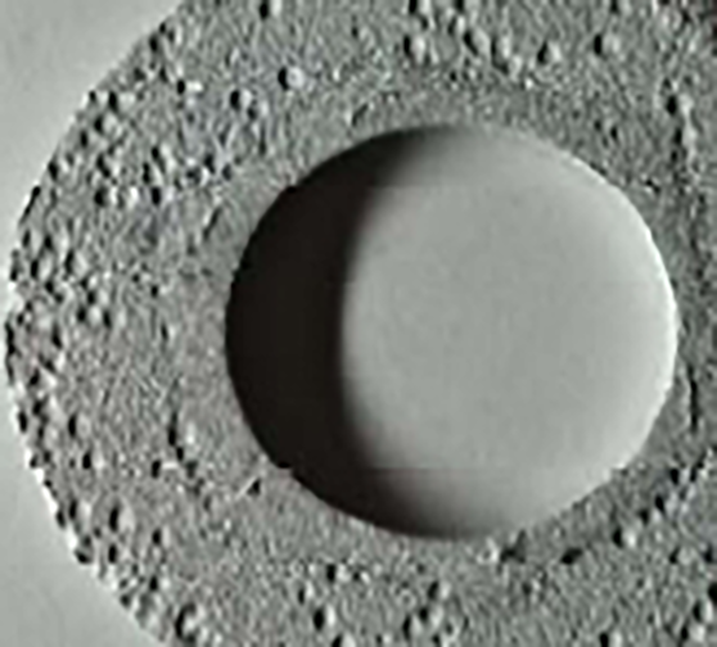
- 上の写真は、鋼板にアルミニウム製ワッシャ(A1050)を樹脂製のボルト、ナットで締付け、5wt%の塩水の入ったバット中に35℃の環境下で500hr浸漬した時に観察された異種金属接触腐食です。
- アルミニウム製ワッシャには孔食が多数観察され、その腐食による重量の減量は、約13%であった。

- 上の写真は、鋼板にアルミニウム製トラスネジ(A5052)を鋼製のボルト、ナットで締付け、5wt%の塩水の入ったバット中に35℃の環境下で500hr浸漬した時に観察された異種金属接触腐食です。
- アルミニウム製トラスネジには孔食が多数観察された。
対策
- 設備や機械の構造は、1種類の金属で構成させる
- 亜鉛などの陽極や外部電源で電気防食する
- 腐食電位の差が小さい材料の組み合わせで使う
- カソード部/アノード部の面積比を小さくする
- 金属面全体を塗装などで被覆し環境遮断する
塗装は、不可避的に欠陥部を有するため、アノード部だけを塗装すると面積比の影響でかえって腐食を早めるで、アノード部だけでなくカソー ド部も塗装する必要がある - 異種金属間の接触部分をゴムや樹脂などで絶縁する
亜鉛の効果
ZAPテープの技術資料の『6.アルミニウム材と鋼板間の異種金属接触腐食に対するZAPシートの効果』の実験に見られるように、亜鉛によって異種金属接触腐食は防止できます。
4.防食方法
材料を腐食から守る方法には下表に示す4つの基本となる防食方法があります。 当社ZAPシリーズは、下記の被覆防食効果、電気防食効果、及び亜鉛が腐食して出来る腐食生成物によるインヒビター効果によって、大切な金属製設備を錆から守ります。
| 分類 | 説明 | 例 | ||
|---|---|---|---|---|
| 被防食材への対応 | 被覆防食 | 被防食材を腐食環境から遮断する方法 | 金属層で被覆 | Crめっき、Snめっき(ブリキ)等 |
| 非金属層で被覆 | 塗装、ライニング、ほうろう等 | |||
| 電気防食 | 被防食材の電位を低下させ防食する方法 | 外部電源方式 | コンクリート構造物の鉄筋や海底掘削装置など | |
| 流電陽極方式 (犠牲陽極方式) |
船体用の亜鉛陽極など | |||
| 材料・構造の最適化 | 被防食材を環境に適合した材質への変更や構造上の腐食要因の除去で防食する方法 | 材料変更 | ステンレス、チタン等への変更 | |
| 構造変更 | 溶接部、隙間等の廃止 | |||
| 腐食環境の制御 | 環境からの腐食要因の除去や環境への腐食抑制物質の添加で防食する方法 | 腐食要因の除去 | 湿度、塩分、亜硫酸ガス、酸素など | |
| 腐食抑制物質の添加 | スルホン酸塩、脂肪族アミン等 | |||
a) 亜鉛による流電陽極方式(犠牲陽極方式)
電気防食のメカニズム 参考:RC構造物におけるZAPシート工法の防食原理
鋼板は、目視では均質に見えても、原子レベルで見るとステップ、キンク、転位など原子配列の乱れが多数あります。このため下図のように水溶液中では低電位の原子配列の乱れた部分がアノードに、その周囲が、電位の高いカソードを形成することで、局部電池が多数形成されます(この場合特にミクロ腐食電池と言います)。この局部電池による電位差でカソード→鋼板→アノード→水溶液と電流が循環し腐食が進行します。
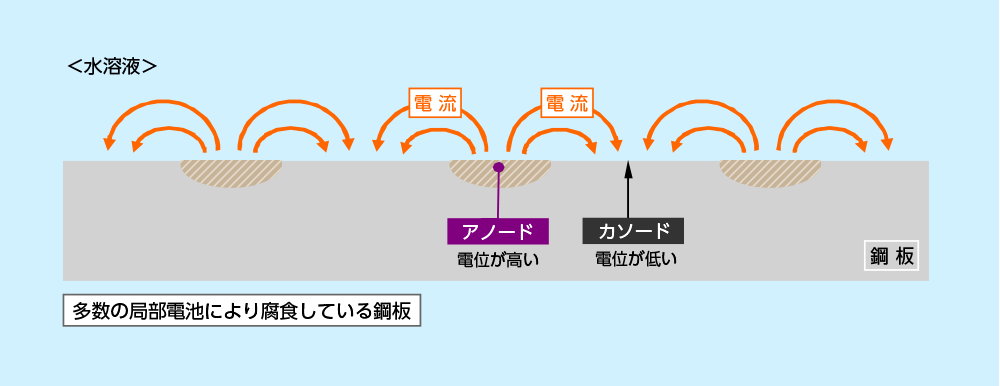
今、上記鋼板に亜鉛板を下図のように電気的に接合すると、両金属間に発生する電位差に基づき、亜鉛が<1式>によって水溶液中に溶解します。この時に発生する電子が、鋼板中で高電位にあるカソードに吸い寄せられ、その電位を低下させます。この電子の供給が十分であれば、鋼板のカソード、アノードの電位差は消失し、鋼板の腐食が停止します。
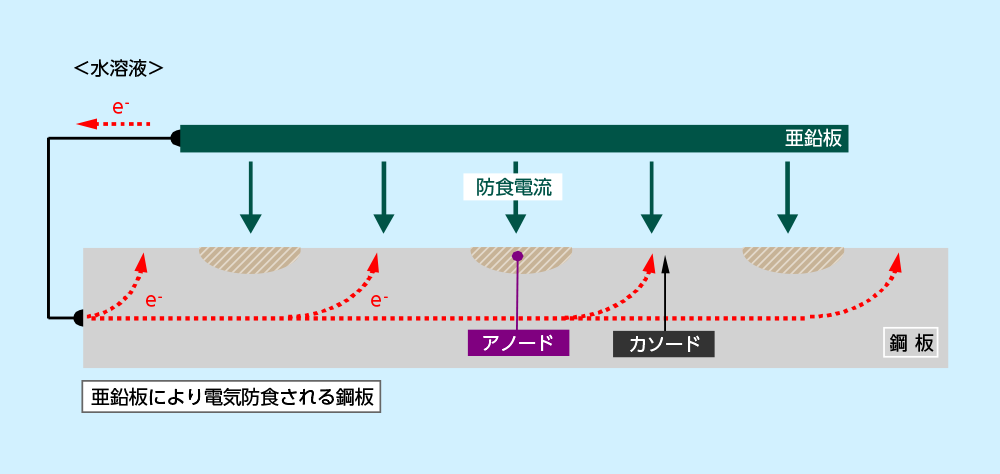
このように電気防食は、外部から電流(電子)を鋼板に供給することで、アノード、カソードの電位差を解消し、腐食を停止させます。
電気防食の種類
電気防食には、被防食体に防食電流を供給する方法により、上記の亜鉛など卑な金属を使用する流電陽極方式(犠牲防食方式とも言う)と、外部に設置した直流電源による外部電源方式があります。
流電陽極方式は、外部電源方式に比べ、
- 直流電源が不要
- 施工が簡単で維持管理が不要
- 過防食による塗膜の剥離、水素脆性の危険性が少ない
- 近接構造物への影響(漏れ電流による腐食)が少ない
等の長所から、多くの場所で使用されています。
亜鉛の効果
下写真は、ブラスト処理した冷間圧延鋼板の中央に純亜鉛板を鋼製ボルトで固定し、水道水に4日浸漬した場合の亜鉛の犠牲防食作用を示しています。
同図より、無防食の鋼板が全面腐食しているのに対し亜鉛板で防食した鋼板は、亜鉛板の周囲の広い範囲に錆が見られず、電気防食が効いていることが確認できます。
- 亜鉛で防食した鋼

- 裸鋼板(無防食品)
